新闻动态
| 祝贺段翼远博士后在Biomaterials上发表论文:手性聚赖氨酸接枝聚氨酯促进巨噬细胞M2型极化 |
| 时间:2020-04-15 11:38 来源:未知 作者:polymer 点击: 次 |
生物材料植入后,宿主的天然免疫系统最先发生响应。当植入材料的性质不理想和/或组织微环境失衡时,会导致局部发生严重的慢性炎症反应。这可能会导致组织修复时间变长甚至无法正常修复(如糖尿病足)或纤维化,致使器官功能部分或全部丧失。修复部位巨噬细胞M1(促炎)和M2(促修复)的极化平衡对组织再生十分重要。通过对材料表界面进行修饰,可以调节植入物引起的巨噬细胞极化平衡、促进功能性组织形成、加速伤口愈合。 由富马酸丙二酯(PPF)二醇和二异氰酸酯(PPFU)合成的不饱和聚氨酯是一种典型的生物降解性热塑性弹性体。富马酸单元的不饱和缺电子双键易于通过Michael加成反应等方法进一步交联或改性。PPFU可以加工成各种形式的材料,在生物医学中有不同的应用。浙江大学高长有、凌君教授团队通过硫醇-烯点击反应将左旋聚赖氨酸(PLL)和右旋聚赖氨酸(PDL)接枝到PPFU薄膜上,发现PLL/PDL接枝修饰的PPFU薄膜(PPFU-g-PLL/PDL),在没有额外细胞因子诱导的情况下,能在体外显著促进骨髓诱导巨噬细胞(BMDM)的M2极化,并能减弱BMDM在LPS和INF-γ诱导的情况下向M1极化的水平。这个发现为提高生物材料的免疫调节能力提供了有效策略和理论指导(图1)。
图1. PLL或PDL接枝到PPFU膜表面调控巨噬细胞极化。
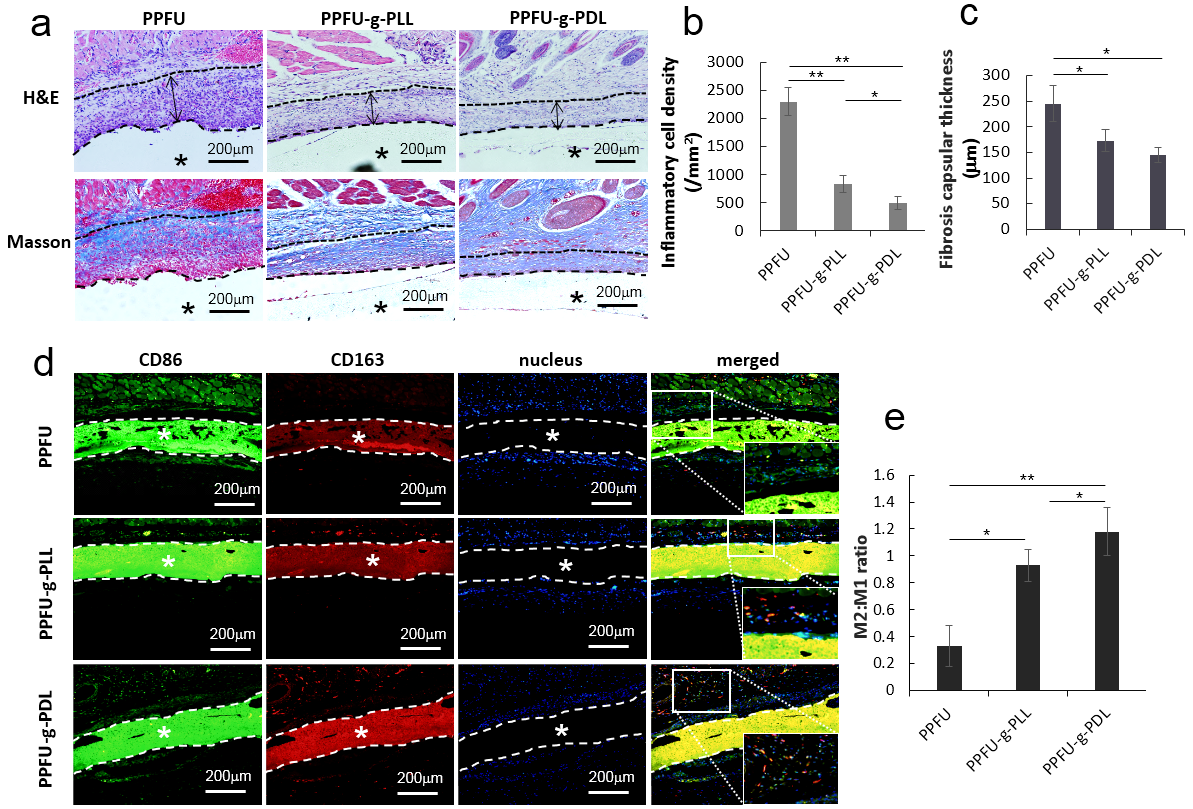
在皮下植入的模型中,PPFU-g-PLL/PDL能够显著上调其周围巨噬细胞M2极化的比例,并有效减少炎症细胞浸润、降低纤维化包膜的厚度(图2)。
图2. 接枝多聚赖氨酸的PPFU膜能够显著减少皮下植入后引起周围组织炎症细胞浸润和纤维包囊厚度,并提高巨噬细胞M2极化的比例。
在上述结果的基础上,研究团队对聚赖氨酸接枝促进巨噬细胞极化的机理进行了进一步挖掘。他们发现可溶性PLL和PDL在低浓度时不会诱导巨噬细胞凋亡或诱导M2极化,而当浓度高于0.2μg/mL时则显著诱导巨噬细胞凋亡,表明聚赖氨酸只有接枝到材料表面才能促进巨噬细胞的M2极化。聚赖氨酸修饰能够显著增加材料表面吸附的蛋白总量并促进BMDM在PPFU膜上的粘附和应力纤维的组装。巨噬细胞很可能通过膜上的CD44和整合素激活粘着斑激酶(FAK)和Rho相关蛋白激酶(ROCK)以及下游的PI3K/Akt1/mTOR信号轴,上调M2相关基因的表达而参与极化过程。
该研究工作“Unsaturated polyurethane films grafted with enantiomeric polylysine promotes macrophage polarization to a M2 phenotype through PI3K/Akt1/mTOR axis”于近日发表在Biomaterials杂志上。论文的第一作者为浙江大学高分子系博士后段翼远,通讯作者为浙江大学高分子系高长有、凌君教授。(论文链接:https://doi.org/10.1016/j.biomaterials.2020.120012)
|